Adsorbsi kimia dan adsorbsi fisika
Adsorpsi adalah merupakan suatu proses yang terjadi ketika suatu fluida (cairan maupun gas) terikat pada padatan dan akhirnya membentuk suatu lapisan tipis pada permukaan tersebut. Contohnya: pembersihan air dengan karbon aktif, dll
(Robert, 1981)
Adsorpsi banyak dijumpai dalam keidupan sehari-hari. Adapun contoh dan peristiwa adsorpsi seperti pada penjernihan air, pemulihan gula, kromatografi, dan dalam bentuk kosmetik, seperti ammonium klorida yang digunakan untuk bahan deodorant yang berfungsi mengadsorpsi protein dalam keringat sehingga menghambat produk dari kelenjar keringat.
(Underwood, 1994)
Ditinjau dari bahan yang
teradsorpsi dan bahan pengadsorben adalah dua fasa yang berbeda, oleh
sebab itu dalam peristiwa adsorbsi, materi teradsorpsi hanya akan
terkumpul dan menempel di permukaan adsorben. Menurut prosesnya adsorpsi ada 2 macam:
Adsorpsi kimia
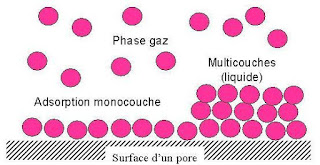
Adsorpsi kimia terjadi karena adanya reaksi antara molekul-molekul adsorbat dengan adsorben, dimana terbentuk ikatan kovalen dengan ion. Adsorbsi ini bersifat tidak reversible dan hanya membentuk lapisan (monolayer). Umumnya terjadi pada temperatur tinggi, sehingga panas adsorpsi tinggi. Adsorpsi ini terjadi dengan pembentukan senyawa kimia, hingga ikatannya lebih kuat. Contoh : adsorpsi O2 pada Hg, HCl, Pt, C.
(Sukardjo, 1997)
Adsorpsi fisika Adsorpsi fisika terjadi apabila gaya intermolekuler lebih besar dari gaya tarik antar molekul atau gaya tarik menarik yang relative lemah antara adsorbat dengan permukaan adsorben. Gaya ini disebut gaya Van Der Waals, sehingga adsorbat dapat bergerak dari satu bagian permukaan ke bagian permukaan lain dari adsorben. Panas adsorpsi rendah, berlangsung cepat, dan kesetimbangan adsorpsi bersifat reversible (dapat bereaksi balik), dan dapat membentuk lapisan jamak (multilayer). Contoh : adsorpsi gas pada choncosl.
(Sukardjo, 1997)
Berdasarkan proses terjadinya ada dua jenis adsorbsi,
yaitu Adsorbsi kimia dan adsorbsi fisika
1. adsorpsi fisika (Physisorption)
Interaksi yang terjadi antara
dasorben dan adsorbat adalah gaya Van der Walls dimana ketika gaya tarik
molekul antara larutan dan permukaan media lebih besar daripada gaya tarik
substansi terlarut dan larutan, maka substansi terlarut akan diadsorpsi oleh
permukaan media. Adsorbsi fisika ini
memiliki gaya tarik Van der Walls yang kekuatannya relatif kecil. Molekul
terikat sangat lemah dan energi yang dilepaskan pada adsorpsi fisika relatif
rendah sekitar 20 kJ/mol.
Contoh : karbon aktif mengikat bau pada
pengolahan air limbah.
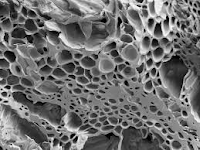
Adsorpsi oleh karbon aktif. Karbon aktif merupakan senyawa karbon yang diaktifkan
dengan cara membuat pori pada struktur karbon tersebut. Aktivasi
karbon aktif pada temperatur yang tinggi akan menghasilkan struktur berpori dan
luas permukaan adsorpsi yang besar. Semakin besar luas permukaan, maka semakin
banyak substansi terlarut yang melekat pada permukaan media adsorpsi.
2. Adsorpsi kimia (Chemisorption)
Chemisorption terjadi ketika terbentuknya
ikatan kimia (bukan ikatan
van Dar Wallis) antara senyawa terlarut dalam larutan dengan molekul
dalam media. Chemisorpsi terjadi diawali dengan adsorpsi fisik, yaitu partikel
adsorbat tertarik
ke permukaan adsorben melalui gaya Van der Walls atau bisa melalui ikatan hidrogen. Dalam Chemisorbption partikel melekat
pada permukaan dengan membentuk ikatan kimia (biasanya ikatan kovalen), dan
cenderung mencari tempat yang memaksimumkan bilangan koordinasi dengan
substrat. Contoh : Ion exchange.
Adsorbat
senyawa terlarut yang dapat terserap
Dalam pengertian lain
menyatakan adsorpsi merupakan suatu peristiwa penyerapan pada lapisan permukaan
atau antar fasa, dimana molekul dari suatu materi terkumpul pada bahan
pengadsorpsi atau adsorben.
zat padat dan zat cair,
Contoh:
karbon aktif mengikat warna anggur merah
zat padat dan gas,
Contoh:
silica gel mengikat air pada desikator
Mengapa adsorben dapat menyerap bahan
lain? Menurut Sukardjo bahwa molekul-molekul pada permukaan zat padat,
mempunyai gaya tarik ke arah dalam, karena tidak ada gaya-gaya yang
mengimbangi. Adanya gaya-gaya ini menyebabkan zat padat dan zat cair, mempunyai
gaya adsorpsi.
Adsorpsi berbeda dengan absorpsi. Pada
absorpsi zat yang diserap masuk ke dalam adsorben sedang pada adsorpsi, zat
yang diserap hanya pada permukaan (Sukardjo, 2002:190). Jumlah zat yang diadsorpsi pada permukaan adsorben merupakan proses
berkesetimbangan, sebab laju adsorpsi disertai dengan terjadinya desorpsi. Pada
awal reaksi, peristiwa adsorpsi lebih dominan dibandingkan dengan peristiwa
desorpsi, sehingga adsorpsi berlangsung cepat. Pada waktu tertentu peristiwa
adsorpsi cenderung berlangsung lambat, dan sebaliknya laju desorpsi cenderung
meningkat. Ketika laju adsorpsi adalah sama dengan laju desorpsi sering disebut
sebagai keadaan berkesetimbangan. Waktu tercapainya keadaan setimbang pada
proses adsorpsi adalah berbeda-beda. Hal ini dipengaruhi oleh jenis interaksi
yang terjadi antara adsorben dengan adsorbat. Secara umum waktu tercapainya
kesetimbangan adsorpsi melalui mekanisme fisika (fisisorpsi) lebih cepat
dibandingkan dengan melalui mekanisme kimia atau kemisorpsi
Perbedaan adsorpsi fisika dan
kimia dapat dilihat pada tabel .
Adsorpsi
fisika
|
Adsorpsi
kimia
|
Molekul terikat pada adsorben
oleh gaya Van der Walls
|
Molekul terikat pada adsorben
oleh ikatan kimia
|
Mempunyai entalpi reaksi -4
sampai -40 kJ/mol
|
Mempunyai entalpi reaksi -40
sampai 800kJ/mol
|
Dapat membentuk lapisan
multilayer
|
Membentuk lapisan Monolayer
|
Adsorpsi hanya terjadi pada
suhu dibawah titik didih adsorbat
|
Adsorpsi dapat terjadi pada
suhu tinggi
|
Jumlah adsorpsi pada permukaan
merupakan fungsi adsorbat
|
Jumlah adsorpsi pada permukaan
merupakan karakteristik adsorben dan adsorbat
|
Tidak melibatkan energi
aktivasi tertentu
|
Melibatan energi aktivasi
tertentu
|
Bersifat tidak spesifik
|
Bersifat sangat spesifik
|

Komentar